„Czy to naprawdę zadziała?”: Młody pacjent z anemią sierpowatą jest jednym z pierwszych, którzy rozpoczęli nową terapię genową
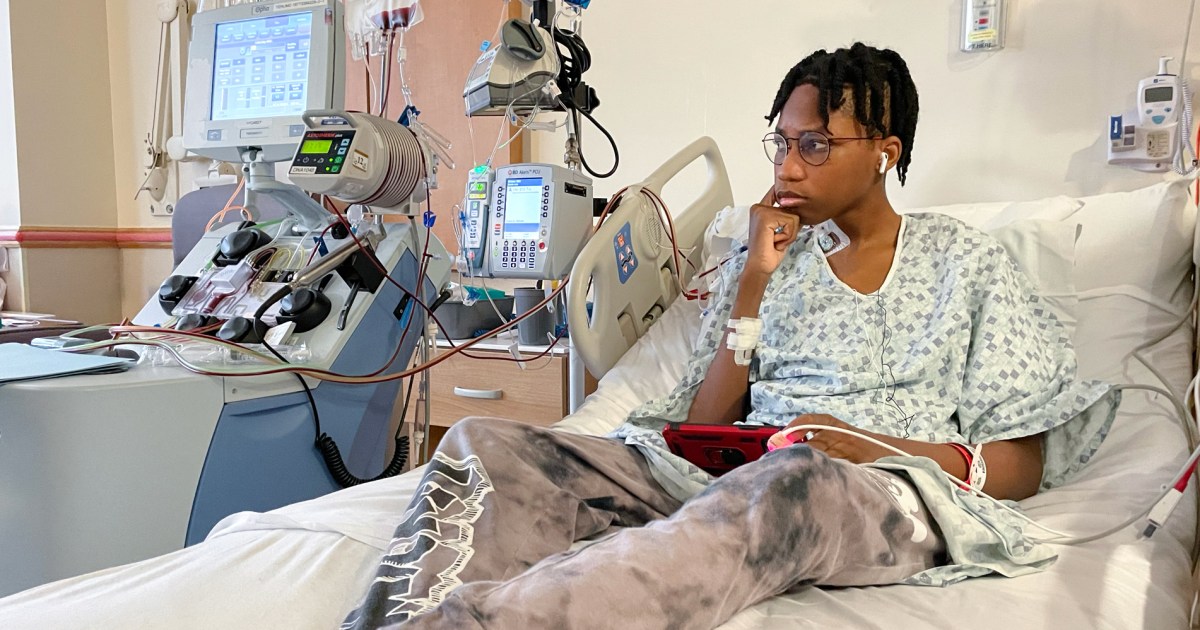
WASZYNGTON — Dla Wedama Minyili sale szpitalne zawsze oznaczały oślepiający ból. „Jakby ktoś wbijał we mnie nóż” – powiedział.
Jednak w niedawny grudniowy poranek 19-letni Wedam, który cierpi na niedokrwistość sierpowatokrwinkową, przez krótką chwilę uwierzył w to, co mówili mu lekarze od miesięcy: ta wizyta może być pierwszym krokiem do wyleczenia. Jako jeden z pierwszych pacjentów na świecie poddany komercyjnemu leczeniu choroby genetycznej mógł zacząć wyobrażać sobie przyszłość wolną od…
„Postanowiłem częściowo w to uwierzyć” – powiedział w dniu przyjęcia do Krajowego Szpitala Dziecięcego w Waszyngtonie w celu pobrania komórek macierzystych, co stanowiło pierwszy ważny krok w rewolucyjnym procesie terapii genowej sierpowatokrwinkowej. „Ale wiąże się to również ze sceptycyzmem: czy to naprawdę zadziała?”
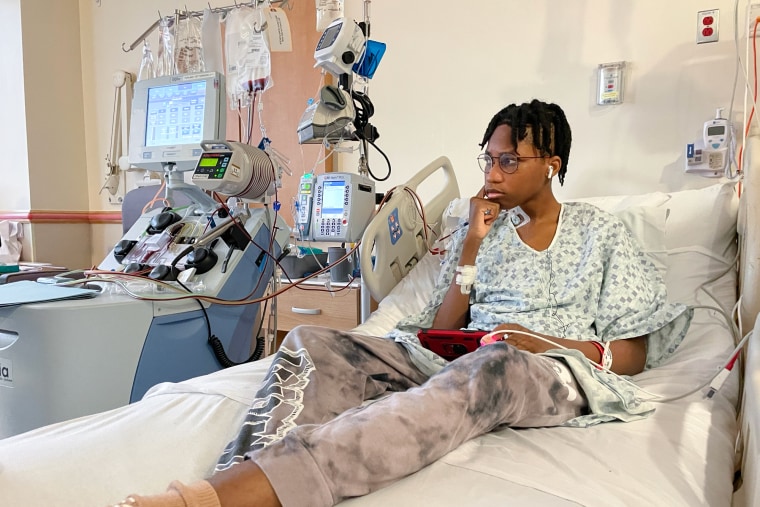
To samo pytanie zadają sobie pacjenci z anemią sierpowatą w całym kraju od chwili, gdy nieco ponad rok temu udało się wyleczyć objawy tej choroby.
Od tego czasu dostęp do niej miało zaledwie kilkudziesięciu pacjentów w całym kraju. Papierkowa robota to katorga, wielomilionowa cena i oznacza, że dotychczas tylko ograniczona liczba szpitali leczyła pacjentów.
Ponad 9 na 10 osób rasy czarnej cierpi na niedokrwistość sierpowatokrwinkową. Dziedziczna choroba powoduje, że czerwone krwinki, zwykle okrągłe, wykrzywiają się w kształt półksiężyca lub sierpa. Komórki sierpowate często gromadzą się w naczyniach krwionośnych, powodując rozdzierający ból, udary, uszkodzenia narządów i krótsze życie. Nowe terapie genowe, jedna firmy Vertex Pharmaceuticals z Bostonu, a druga firmy Bluebird Bio z Somerville w stanie Massachusetts, oferują potencjalne lekarstwo.
Właśnie dlatego Wedam przełamał swój sceptycyzm i przez miesiące pracował nad uzyskaniem zezwoleń ubezpieczeniowych i konsultacji lekarskich.
„Wiem, co to może dla mnie oznaczać” – powiedział cicho, gdy zespół lekarzy zaczął tłoczyć się przy jego łóżku. „Ale dopóki to się nie stanie, nie jestem tak podekscytowany jak wszyscy inni”.
Jego mama, Sylvia, przyglądała się temu z rogu pokoju, wstrzymując oddech. „To coś zupełnie nowego” – stwierdziła. „I nigdy nie myślałem, że, wiesz, będziemy jednym z pionierów w tym zakresie. Wydaje się to nierealne.”
Ale pierwszy etap tego, co opisuje jako „cud”, wydarzył się na jej oczach: pielęgniarki podały jej synowi lek, który miał zmobilizować komórki macierzyste normalnie uwięzione w szpiku kostnym i przedostać się do krwioobiegu. Kilka godzin później Wedam został podłączony do tak zwanej maszyny do aferezy, która pobiera krew z organizmu, a następnie wiruje ją z dużą prędkością, aby oddzielić miliony komórek macierzystych, zanim reszta krwi zwróci resztę krwi do krwiobiegu. słojowanie.
Doktor Andrew Campell podszedł do łóżka Wedama, gdy do wiszącej obok niego torebki kroplowej zaczęła zbierać się pierwsza jasnopomarańczowa ciecz zawierająca jego komórki macierzyste.
„Jesteście jedną z nielicznych w kraju, a nawet na świecie, podejmujących ten ważny krok — terapię genową” – powiedział Campbell, dyrektor szpitalnego kompleksowego programu niedokrwistości sierpowatokrwinkowej. „Wymagało to dużej odwagi, ponieważ wiem, że jest to wciąż coś nowego”.
Wedam wyglądał na niewzruszonego. „Musiałem” – powiedział. „Tak naprawdę nie ma czegoś, co mógłbym przepuścić. Więc tak naprawdę nie miałem wyboru.
Krzywa uczenia się dla szpitali
W nadchodzących miesiącach komórki Wedama zostaną wysłane do laboratorium w Tennessee, gdzie technicy wykorzystają modyfikację genu w komórkach macierzystych, tak aby wytwarzały czerwone krwinki, które są mniej podatne na sierpowanie i blokowanie przepływu krwi, co skutkuje…
Wedam będzie potrzebował intensywnej chemioterapii, aby zniszczyć istniejące komórki macierzyste i zrobić miejsce w szpiku kostnym dla komórek poddanych edycji genów, które zespół z Krajowego Szpitala Dziecięcego ponownie wprowadzi dożylnie do jego krwiobiegu.
„Możliwość zapewnienia terapii, która wyleczy, uchroni go przed szpitalem i prawdopodobnie przedłuży życie, to coś niesamowitego” – powiedział dr David Jacobsohn, szef działu przeszczepów krwi i szpiku w Children’s National. „To, co jesteśmy w stanie zapewnić teraz, w porównaniu z pięcioma czy 10 latami temu, jest bardzo, bardzo potężne”.

Mimo to Jacobsohn przyznał, że niewielu pacjentów rozpoczęło terapię genową. W firmie Children’s National, która wyprzedziła konkurencję po wzięciu udziału w badaniach klinicznych Bluebird Bio, tylko 10 osób, w tym Wedam, rozpoczęło lub zakończyło ten proces. To dane z puli około 1500 pacjentów z niedokrwistością sierpowatokrwinkową, których zespół leczy w rejonie Waszyngtonu.
„Na początku, gdy kierownictwo szpitala było bardzo podekscytowane, byli bardzo podekscytowani. Powiedzieli: „Mamy kilkudziesięciu kwalifikujących się pacjentów. Musimy zbudować więcej łóżek! Mam wrażenie, że w końcu to zrobimy, ale nie stanie się to od razu” – powiedział. „To była lekcja uczenia się dla szpitali i dla firm ubezpieczeniowych”.
Jacobsohn powiedział, że jego zespół pracuje nad rozpoczęciem leczenia u jednego lub dwóch pacjentów miesięcznie – tempo, które określił jako „ekscytujące”.
„Pamiętajcie, że jest to leczenie bardzo wysokiego ryzyka, wymagające chemioterapii w dużych dawkach i mogące powodować powikłania” – powiedział. „Nie jest to więc coś, co chcielibyśmy przyspieszyć.”
Miesięczna kuracja Casgevy firmy Vertex Pharmaceuticals kosztuje 2,3 miliona dolarów. Lyfgenia firmy Bluebird Bio jest wyceniana na 3,1 miliona dolarów. Nie obejmuje to kosztów opieki związanej z pobytem w szpitalu ani chemioterapią.
Aby poradzić sobie z wysoką ceną, ubezpieczyciele wdrożyli obszerne procedury preautoryzacji. Obie firmy farmaceutyczne powiedziały NBC News, że nie spotkały się jeszcze z „ostateczną odmową” ich leków.
Jacobsohn powiedział, że procedura wymaga dużych zasobów w przypadku ograniczonej liczby szpitali uprawnionych do jej przeprowadzania, wymaga wielodniowego pobytu w szpitalu w celu pobrania komórek macierzystych, a kilka miesięcy później wielotygodniowego pobytu w szpitalu w celu chemioterapii i ponownego wprowadzenia komórek macierzystych. W międzyczasie laboratorium przetwarzające komórki macierzyste potrzebuje kilku miesięcy na genetyczną modyfikację komórek i przeprowadzenie kontroli bezpieczeństwa, zanim odeśle je z powrotem do szpitala w celu infuzji.
W przypadku pacjentów takich jak Wedam istnieją również inne względy. Intensywna chemioterapia trwa cztery dni i powoduje, że pacjenci są wyjątkowo chorzy i podatni na infekcje. U wielu osób rozwijają się wrzody w jamie ustnej, gardle i przełyku, które uniemożliwiają jedzenie. W dłuższej perspektywie chemioterapia zwiększa ryzyko raka i .
Z tych wszystkich powodów tylko jeden pacjent zakończył proces w Centrum Onkologii Dziecięcej City of Hope w Los Angeles. Doktor Leo Wang, hematolog-onkolog dziecięcy pracujący w ośrodku, twierdzi, że spodziewa się szybkiego wzrostu tej liczby w nadchodzących miesiącach, gdy „pierwsi użytkownicy” zaczną odnosić sukcesy.
„Mamy wielką nadzieję, że zainteresowanie wzrośnie i stanie się bardziej akceptowalne dla osób, które być może mają nieco większą niechęć do ryzyka” – powiedział Wang. „Widzieliśmy już, że pacjenci przychodzą, pytają nas o to i mówią: «No cóż, naprawdę chciałbym porozmawiać z kimś, kto już przez to przeszedł i poznać jego punkt widzenia, a wtedy może uda mi się». będę zainteresowany zrobieniem tego.”
„Boże, zrobiłeś to dla mnie”
To jedna z motywacji Wedama, aby zostać „wczesnym użytkownikiem”. „Gdyby wszyscy ci ludzie mogli mnie zobaczyć i przekonać się, że to działa, mieliby jakąś nadzieję” – powiedział. „Nawet jeśli to trochę.”
Choroba pozbawiła go możliwości zrobienia praktycznie wszystkiego, łącznie ze wstawaniem z łóżka. Ale pomysł na lekarstwo sprawił, że marzy o tym, by pewnego dnia zostać filmowcem.
W najbliższej perspektywie jego ambicje są znacznie mniejsze — wolałby uczestniczyć w zajęciach w college’u osobiście, a nie online.
„Teraz nie dotrzymuję kroku większości moich znajomych, więc mógłbym poznać nowych” – powiedział. „Byłbym w stanie lepiej nauczyć się materiału, gdybym był osobiście i zadawał nauczycielowi konkretne pytania. Po prostu myślę, że bycie normalną osobą i robienie tego, co zrobiłby normalny człowiek, właśnie to mnie naprawdę ekscytuje.
Choroba pustoszyła rodzinę Minyila przez prawie dwie dekady. Oprócz Wedama na anemię sierpowatą choruje także jego 14-letni brat Wekem.

„Zabrano prawie wszystko” – stwierdziła Sylvia Minyila. „Odebrano nam radość”.
Wedam, powiedziała, był kiedyś szczęśliwym chłopcem, który kochał szkołę i taniec. Ale kiedy w gimnazjum zaczęły się jego kryzysy bólowe, powiedziała, zmienił się.
„Stał się wycofany. Gdziekolwiek była kość, mógł odczuwać ból” – powiedziała. „Gdziekolwiek w domu byłeś, słyszałeś jego jęki. I to jest coś, o czym regularnie myślałem: „Czy go stracę?” Ponieważ bardzo cierpiał.”
Do czasu terapii genowej jedynym lekarstwem na anemię sierpowatokrwinkową był przeszczep komórek macierzystych od dawcy. To zadziałało w przypadku Wekema, gdy Sylvia odkryła, że pasuje do jej młodszego syna. Po strasznych komplikacjach zabieg się udał.
Jednak przeciwciała w krwiobiegu Wedama uniemożliwiły mu wyleczenie.
„Byłem zachwycony. Powiedziałam: „Boże, zrobiłeś to dla mnie”. A co z moim drugim synem?” – zapytała Sylvia ze łzami w oczach. „Chciałem tego samego dla Wedama”.
Powiedziała, że kiedy zaledwie kilka miesięcy później lekarze ze Szpitala Dziecięcego zadzwonili do niej i poinformowali, że Wedam może być dobrym kandydatem do nowej terapii genowej, wydawało jej się to podwójnym cudem — odpowiedzią na jej modlitwy.
„Zapytywałem tylko: «Czy to leczy? Czy z tego powodu nadal będzie musiał brać leki? Czy będzie miał ataki bólowe? Powiedzieli: „Nie”. A ja powiedziałem: „Weszliśmy w to. Weszliśmy w to”.
Wedam widział, jak jego młodszy brat zmienił się od czasu leczenia – nawet wykorzystując nową energię, aby nauczyć się jeździć na rowerze. Rozdzierający ból przed przeszczepieniem komórek macierzystych Wekema uniemożliwił to.
Wekem powiedział, że nie może się doczekać uzdrowienia swojego starszego brata.
„Czuję, że to zmieniło jego życie, jakie będzie prowadził” – powiedział Wekem. „Naprawdę nie sądziłam, że będzie dla nas dostępne coś innego, co umożliwiłoby mu leczenie i wyleczenie”.
Wedam pozostaje jednak sceptyczny. „Może 60%” – powiedział o swoich szansach na wyleczenie.
Jednak nawet biorąc pod uwagę zagrażające życiu komplikacje, które mogą wystąpić, powiedział, jeśli istnieje jakakolwiek szansa na mniej bolesną przyszłość, warto spróbować.
NBC News będzie w dalszym ciągu śledzić podróż Wedama Minyili, gdy rozpoczyna on kolejne etapy leczenia anemii sierpowatokrwinkowej.